来源于传染病预防控制国家重点实验室
反向人兽共患病的英文是reverse zoonotic disease,是指人类把病原体传给动物,引起动物发病。大量野生、规模化养殖、圈养动物等因与人类密切接触的机会增加,而被人传染,即反向人兽共患病。有专家统计,过去70年,和人类农业生产活动相关的病毒性人兽共患新发传染病占到新发传染病的50%以上;人类与猪、牛、马、狗、猫、羊交流的病毒分别有31种、31种、31种、27种、16种、22种之多。已经发表的关于反向人兽共患病的论文呈逐年增多之势[1, 2]。但是,这些已经报道的反向人兽共患病多是偶然发生的事件[1],基本上是人感染了一种动物的病原体后,在一定的条件下,可把病原体传给其他动物,特别是养殖动物。
南开大学公共卫生与健康研究院、中国疾病预防控制中心传染病预防控制国家重点实验室徐建国院士团队关于福氏志贺菌人传牛研究最近在Emerging Microbes & Infections 杂志在线发表,在世界范围内首次发现人类可把志贺氏菌传给牦牛、肉牛、奶牛等。多少年来,学术界一致认为志贺菌是人类特有的病原菌,人是唯一宿主[3]。过去我们常说,70%以上的新发传染病来自动物。这个发现,对认识新发传染病是如何发生的,引起动物的疾病具有重要启发意义。
细菌性痢疾是与贫穷、卫生条件差、无干净水源和食品等密切相关的传染病,改革开放之前非常多见。中国最常见的是福氏志贺氏菌。每年全球感染志贺氏菌的人数约有1.647 亿,导致约 110 万人死亡,其中95%的致死病例发生在发展中国家。
中国农业科学院兰州畜牧与药物研究所的科学家于2014年至2016年从甘肃、青海、陕西等地的肉牛、牦牛粪便样本中分离到福氏志贺氏菌。在深入研究的34株福氏志贺菌中,16株来自牦牛,10株来自奶牛,8株来自肉牛。牦牛、奶牛和肉牛的检出率分别为1.22%(16/1311)、2.11%(10/474)和2.52%(8/317)。大多数分离自(61.76%,21/34)腹泻犊牛。
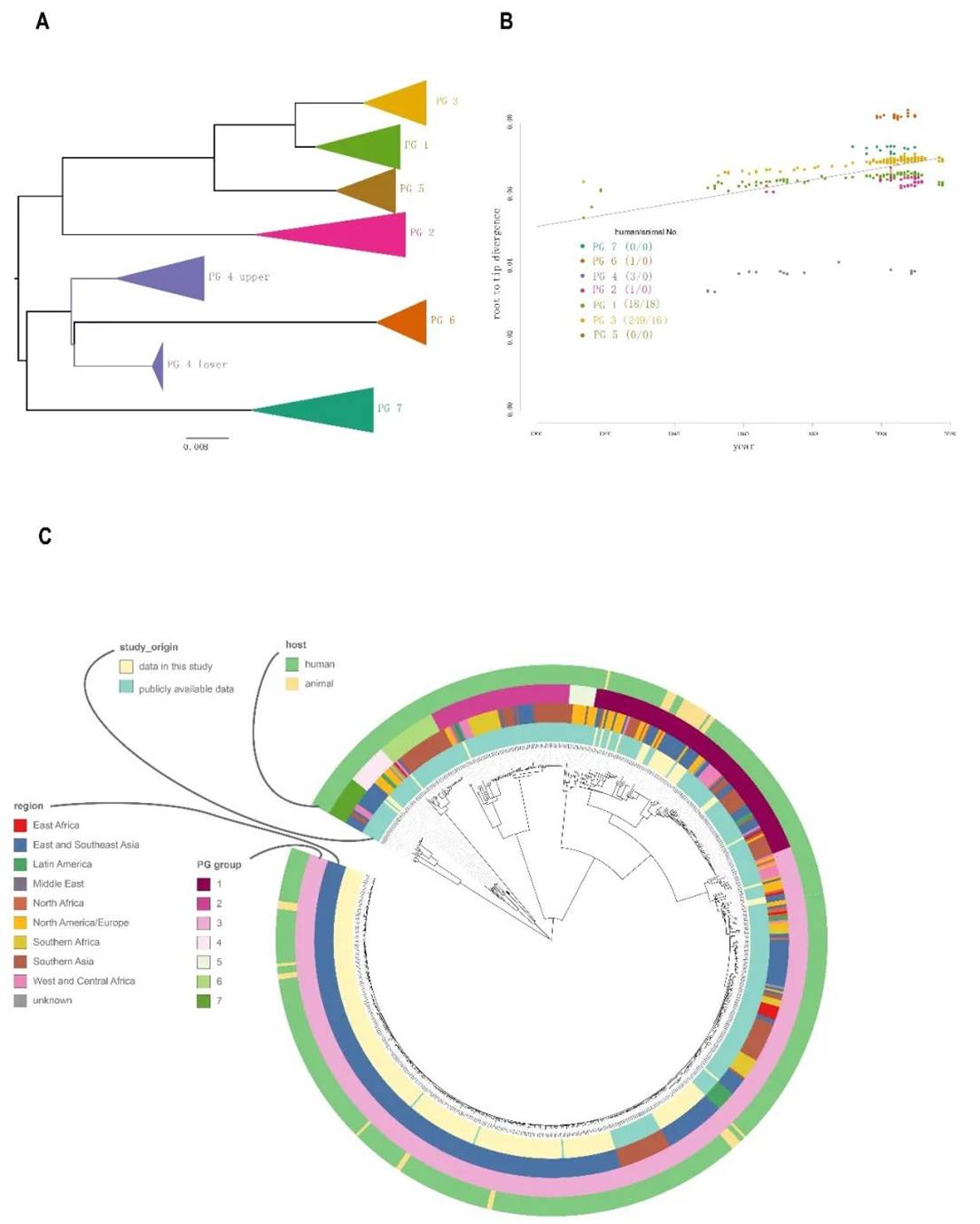
徐建国院士团队和中国医学科学院苏州系统医学研究所、北京师范大学、澳大利亚新南威尔士大学和河北工程大学等多个团队合作,对从牦牛奶牛肉牛分离34株动物菌株,和1950至2017年间从17个省市患者分离的268株进行了基因组测序,结合全球公共数据库的346株福氏志贺氏菌基因组序列,一起进行系统发生学分析。研究发现,可把这648株福氏志贺菌分为7个PG群 (图1)。34株动物志贺菌可分为2个群,PG1和PG3,分别占52.94%(18/34)和 47.06%(16/34)。从系统发生学信息看,PG1群菌株显现时间早,主要为牦牛分离株;PG3菌株显现时间晚,主要为肉牛和奶牛分离株。中国患者菌群主要是PG3群,占91.54%(249/272)。在毒力质粒、抗菌素耐药基因等方面,PG1和PG3菌株具有明显的差异。PG3动物分离株与近年来在中国人群中的流行株相似,均为ST91型,具有多重耐药特点,部分属于近年新出现的Xv血清型。
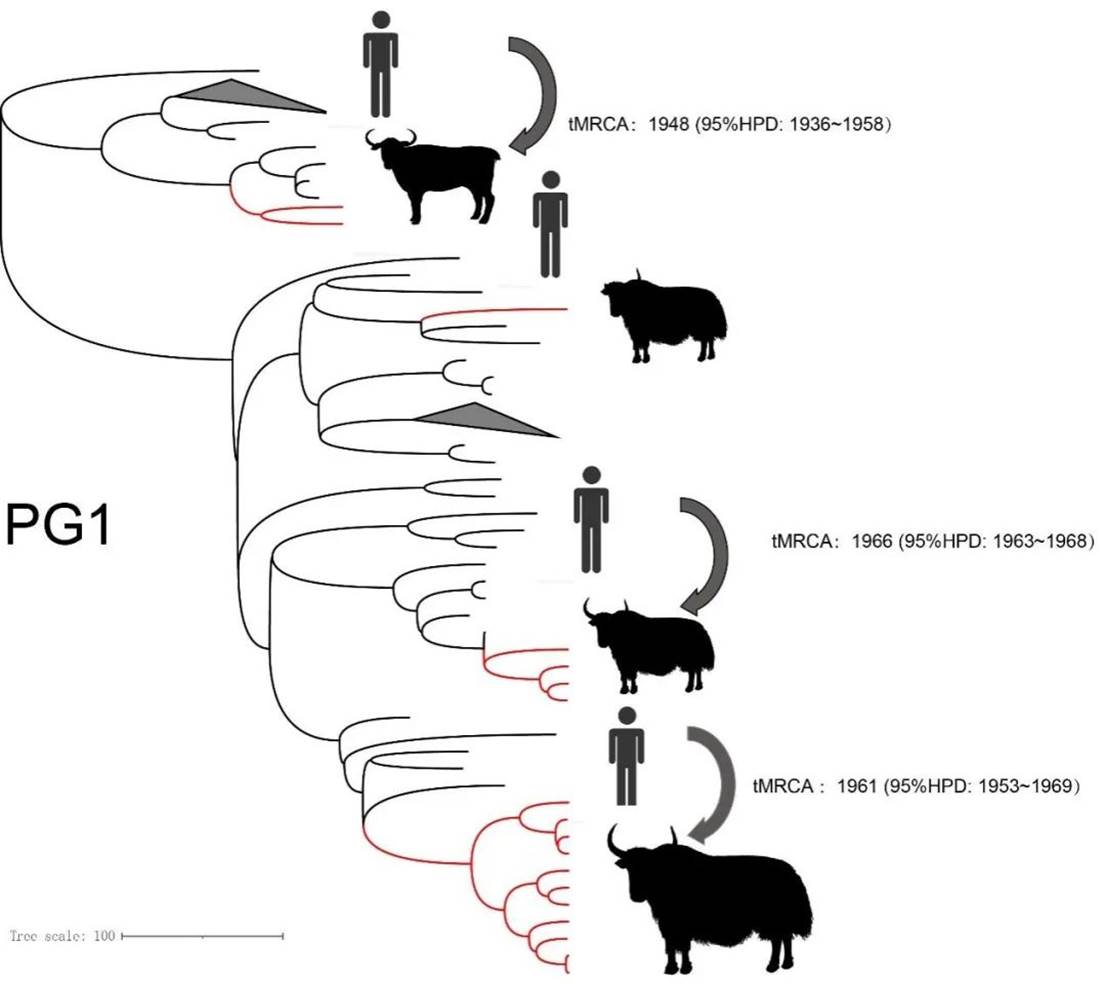
PG1种群的最早显现的时间大约为1660年左右,PG3种群的最早显现时间大约为1848年左右。在PG1和PG3菌株的系统发生树上,人类菌株处于祖先的位置,充分提示是人把志贺菌传给牛的。采用 BEAST 软件对不同宿主种群进行系统发育分析和分化时间估计,结果显示PG1动物菌株可分为4个谱系,显现时间估计在1948-1966年之间;PG3菌株可分为8个谱系,显现的时间估计为1997-2016年(图2,图3)。也就是说,人类把志贺菌传给牛的时间大约在上述年代,且发生了多次。在志贺菌从人传给牛后,福氏志贺氏菌种群进化速率有显著差异,进化速率减慢。
有意思的是,福氏志贺氏菌引起的细菌性痢疾属于夏季高发,病人多在5-10月之间出现,这是过去腹泻病门诊工作的时间。可是,引起牛的腹泻,多是冬季发生。菌株主要是10-12-3月份分离的。天寒地冻,采样时还要穿着羽绒服。
本研究的局限性是动物分离株较少,收集时间较短,可能对分析结果造成偏倚。对于已经适应动物的病原体,成为人类病原体之前,必须要克服一些行为屏障,即增加和人类接触的机会。所幸到目前为止还未发现福氏志贺氏菌从牛回传再次感染人的情况出现。
本研究的重要意义在于,许多传染病是行为生态型传染病,人类活动,特别是规模化经济社会活动,不仅可以导致病原体从动物传给人,引起人间疫情,如SARS;同时,也可导致病原体从人传给动物,导致动物传染病的发生。
文章以Evolutionary and genomic insights into the long-term colonization of Shigella flexneri in animals为题发表于2022年8月Emerging Microbes & Infections,中国疾病预防控制中心传染病所梁俊容博士、河北工程大学朱阵博士、澳大利亚新南威尔士大学兰瑞廷教授、中国医学科学院苏州系统医学研究所孟静博士和比利时鲁汶大学Bram Vrancken博士为文章共同第一作者,徐建国院士和蒋太交研究员为共同责任作者[3]。国内外4个团队共同完成。

参考文献
1. Messenger AM, Barnes AN, Gray GC: Reverse zoonotic disease transmission (zooanthroponosis): a systematic review of seldom-documented human biological threats to animals. PLoS One 2014, 9(2):e89055.
2. Glud HA, George S, Skovgaard K, Larsen LE: Zoonotic and reverse zoonotic transmission of viruses between humans and pigs. APMIS 2021, 129(12):675-693.
3. Liang J, Zhu Z, Lan R, Meng J, Vrancken B, Lu S, Jin D, Yang J, Wang J, Qin T et al: Evolutionary and genomic insights into the long-term colonization of Shigella flexneri in animals. Emerg Microbes Infect 2022:1-67.



